Items 222 & 223 – Facteurs de risque cardiovasculaire, prévention – Dyslipidémies
________________________________________________________________________
Situations de départ
- 42 Hypertension artérielle.
- 51 Obésité et surpoids.
- 57 Prise de poids.
- 195 Analyse du bilan lipidique.
- 207 Ferritine : baisse ou augmentation.
- 208 Hyperglycémie.
- 252 Prescription d’un hypolipémiant.
- 266 Consultation de suivi d’un patient polymédiqué.
- 279 Consultation de suivi d’une pathologie chronique.
- 280 Prescription d’une insulinothérapie, consultation de suivi, éducation d’un patient diabétique de type 1.
- 281 Prescription médicamenteuse, consultation de suivi et éducation d’un patient diabétique de type 2 ou ayant un diabète secondaire.
- 282 Prescription médicamenteuse, consultation de suivi et éducation d’un patient hypertendu.
- 285 Consultation de suivi et éducation thérapeutique d’un patient avec un antécédent cardiovasculaire.
- 320 Prévention des maladies cardiovasculaires.
- 352 Expliquer un traitement au patient (adulte, enfant, adolescent).
- 354 Évaluation de l’observance thérapeutique.
________________________________________________________________________________
________________________________________________________________________________
Hiérarchisation des connaissances
________________________________________________________________________________
Item 222 – Facteurs de risque cardiovasculaire, prévention
______________________________________________________________________________
| Rang | Rubrique | Intitulé |
| A | Définition | Définition de la prévention cardiovasculaire primaire, secondaire et primo-secondaire |
| A | Définition | Facteurs de risque majeurs, indépendants, modifiables (tabac, HTA, diabète, dyslipidémie) et non modifiables (âge, sexe masculin, hérédité) |
| A | Définition | Agrégation de facteurs de risque et facteurs de risque indirects (obésité, sédentarité, syndrome métabolique) |
| A | Définition | Stratégies individuelles de prévention : mesures hygiéno-diététiques et traitements médicamenteux |
| A | Prévalence, épidémiologie | Prévalence, risque cardiovasculaire associé et pourcentage de pathologies cardiovasculaires évitables en cas de prise en charge des facteurs de risque majeurs modifiables (HTA, tabac, diabète, dyslipidémie), connaître l’existence de scores (sans savoir le calculer) |
| B | Éléments physiopathologiques | Rôle de l’alcool dans le risque cardiovasculaire |
| B | Éléments physiopathologiques | Rôle des facteurs psychosociaux dans le risque cardiovasculaire |
| B | Éléments physiopathologiques | Rôle de l’hypertriglycéridémie dans le risque cardiovasculaire |
| B | Étiologie | Expliquer l’influence de l’excès de poids dans le risque cardiovasculaire |
| A | Prise en charge | Connaître le bénéfice de l’activité physique pour la prise en charge du risque cardiovasculaire |
| B | Prise en charge | Décrire la quantité d’activité physique à conseiller en prévention cardiovasculaire primaire |
| A | Suivi et/ou pronostic | Connaître l’efficacité de la prévention cardiovasculaire centrée sur le patient en soins primaires |
________________________________________________________________________________
Item 223 – Dyslipidémies
________________________________________________________________________________
| Rang | Rubrique | Intitulé | Descriptif |
| A | Définition | Évaluation du risque cardiovasculaire global | |
| A | Définition | Connaître les trois grands types de dyslipidémies | Hypercholestérolémie pure, hypertriglycéridémie pure, hyperlipidémie mixte |
| B | Éléments physiopathologiques | Connaître les relations entre lipides et athérosclérose | |
| A | Dépistage | Quand dépister une dyslipidémie ? | |
| A | Diagnostic positif | Diagnostic positif et classification des dyslipidémies | Exploration d’une anomalie lipidique, valeurs seuils, classification simplifiée |
| A | Contenu multimédia | Connaître les manifestations cliniques des dyslipidémies : xanthélasma | |
| A | Étiologie | Connaître les principales causes d’hyperlipidémies secondaires | Endocrinopathies, maladies rénales, atteintes hépatiques, médicaments |
| B | Examens complémentaires | Quel bilan biologique faire à la recherche d’une dyslipidémie secondaire | |
| A | Prise en charge | Connaître les principes du traitement des dyslipidémies | |
| A | Prise en charge | Connaître les règles hygiénodiététiques | Recommandations diététiques adaptées en cas de dyslipidémies |
________________________________________________________________________________
Facteurs de risques cardiovasculaire, prévention – Dyslipidémies
- Définitions
- Facteurs de risque à prendre en compte
- Tabac
- Hyperlipidémies
- Hypertension artérielle et risque cardiovasculaire
- Diabète et risque cardiovasculaire
- Prise en charge du risque cardiovasculaire
I Définitions
A Notion de facteur de risque
Il s’agit d’une situation associée à une majoration du risque de survenue de complications cardiovasculaires ischémiques. Il peut s’agir :
- d’un état physiologique (vieillissement, ménopause) ;
- d’un état pathologique (HTA, diabète, obésité abdominale) ;
- d’une habitude de vie (tabagisme, sédentarité).
S’il existe un lien de causalité directe entre l’agent et la maladie, il s’agit d’un authentique « facteur de risque ».
Pour que le facteur de risque soit cliniquement pertinent, il doit satisfaire plusieurs conditions :
- intensité de la relation ;
- gradient de risque élevé pour chaque écart type de variation du facteur ;
- relation dose-effet : le risque de développer la maladie augmente proportionnellement selon le niveau d’exposition au facteur de risque ;
- indépendance : l’association entre le facteur de risque et la maladie persiste quel que soit le niveau des autres facteurs de risque — la relation persiste en analyse multivariée ;
- concordance : association établie par plusieurs études épidémiologiques convergentes ;
- séquence temporelle : l’exposition au facteur de risque précède la maladie ;
- cohérence physiopathologique : caractère plausible de l’association sur des données expérimentales ;
- réversibilité : la correction du facteur de risque lors d’études contrôlées permet de prévenir la maladie ou d’en réduire l’incidence ; cette démonstration essentielle établit formellement la preuve de la causalité.
B Prévention primaire et secondaire
1 Prévention primaire
La prévention primaire consiste à éviter la survenue ultérieure d’un accident cardiovasculaire en corrigeant les facteurs de risque identifiés chez des patients indemnes de tout événement cardiovasculaire.
2 Prévention secondaire
La prévention secondaire consiste à éviter la survenue d’un accident cardiovasculaire chez des patients ayant déjà présenté un accident cardiovasculaire en corrigeant les facteurs de risque identifiés et en agissant sur la maladie cardiovasculaire constituée.
La notion de prévention secondaire et primaire est complétée par le classement des patients en fonction du risque cardiovasculaire (cf. infra).
Les patients en prévention secondaire sont par définition à haut risque cardiovasculaire ou à très haut risque dans les nouvelles recommandations européennes. Il existe des situations où les patients sont à haut risque mais en prévention primaire ; c’est le cas par exemple des patients qui ont une sténose de la carotide supérieure à 50 % ou un cumul de facteur de risque exceptionnel.
II Facteurs de risque à prendre en compte
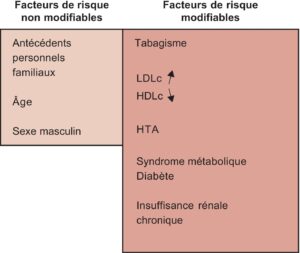
Les facteurs de risque cardiovasculaire modifiables et non modifiables sont représentés dans la figure 1 (Afssaps, 2005).
________________________________________________________________________________
Fig. 1.
Présentation synthétique des principaux facteurs de risque cardiovasculaire.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
A Facteurs de risque non modifiables
Ils doivent être pris en considération car ils déterminent puissamment le niveau de risque absolu et donc l’amplitude du bénéfice absolu après une intervention :
- homme âgé de 50 ans ou plus ;
- femme âgée de 60 ans ou plus ou ménopausée ;
- antécédents familiaux de maladie coronarienne précoce :
- infarctus du myocarde ou mort subite avant l’âge de 55 ans chez le père ou le frère ;
- infarctus du myocarde ou mort subite avant l’âge de 65 ans chez la mère ou la sœur.
B Facteurs de risque modifiables
Leur identification participe à l’estimation du risque et ce sont eux qui constituent la cible des actions de prévention :
- tabagisme en cours (dès 1 cigarette par jour ou sevré depuis moins de 3 ans) ;
- hypercholestérolémie avec LDL-cholestérol (LDL-c) élevé ;
- HDL-cholestérol (HDLc) inférieur à 0,40 g/l [1 mmol/l], quel que soit le sexe ;
- hypertension artérielle ;
- diabète, traité ou non, et syndrome métabolique (cf. infra) ;
- insuffisance rénale chronique.
À l’inverse, le HDL-cholestérol supérieur ou égal à 0,60 g/l [1,5 mmol/l] constitue un facteur de protection : soustraire alors « un risque » à la somme des facteurs de risque cardiovasculaire.
C Méthodes d’estimation du risque vasculaire individuel
1 Concept
L’estimation du risque vasculaire du sujet consiste à recenser l’ensemble des facteurs de risque cardiovasculaire — ils ont un caractère multiplicatif — et à déduire ainsi la probabilité de survenue d’une complication ischémique. Les facteurs de risque ont un effet synergique sur le niveau de risque.
L’estimation du risque peut être quantitative, exprimée en probabilité de présenter une complication en 10 ans, en employant des équations multifactorielles. Le principe de ces équations est d’éliminer les facteurs redondants. De nombreuses équations sont utilisables. L’équation la plus connue est celle tirée de l’étude de Framingham (États-Unis), pour laquelle des modèles récents ont été proposés. Cette équation a tendance à surestimer le risque dans les pays à bas risque.
L’équation européenne issue du projet SCORE concerne les pays à faible incidence de complications cardiovasculaires, mais elle n’estime que la mortalité cardiovasculaire (fig. 2) ; la mortalité représente 30 % de la globalité des événements ischémiques. C’est cette équation qui a été retenue en France pour classifier le risque cardiovasculaire.
________________________________________________________________________________
Fig. 2.
Table SCORE (Systematic COronary Risk Evaluation) : risque de décès cardiovasculaire en 10 ans (table pour les régions d’Europe dite à « faible risque », dont la France).
(Source : European Guidelines on CVD Prevention in Clinical Practice 2016. Eur J Prev Cardiol 2016 ; 23(11) : NP1–96 (version 2016). With permission of Oxford University Press (UK) © European Society of Cardiology, www.escardio.org/guidelines.)

________________________________________________________________________________
2 Estimation du risque en pratique
Interrogatoire
L’interrogatoire consiste à :
- recueillir des antécédents familiaux cardiovasculaires ;
- rechercher des antécédents personnels ischémiques ou des signes fonctionnels évocateurs tels qu’angor, AOMI (artériopathie des membres inférieurs), AIT (accident ischémique transitoire) ;
- recueillir des facteurs de risque cardiovasculaire.
Examen
L’examen consiste à :
- rechercher un athérome asymptomatique : pouls périphérique, souffles vasculaires ;
- rechercher un athérome infraclinique :
- ECG basal : recherche de troubles de repolarisation, de séquelles de nécrose, d’hypertrophie ventriculaire gauche électrique ;
- échographie de la carotide : la mesure de l’épaisseur intima-média de la carotide et la recherche systématique de plaques ne sont pas recommandées en pratique courante dans la stratification du risque.
3 Estimation du risque absolu (défini par la probabilité de présenter la maladie dans un laps de temps donné)
Elle repose sur l’utilisation d’équations ou de tables ou la simple sommation des facteurs de risque cardiovasculaire :
- un risque d’événement voisin de 10 % à un horizon de 10 ans est considéré comme faible ;
- un risque supérieur à 20 % est considéré comme important — c’est le niveau de risque coronarien observé dans les suites d’un infarctus du myocarde ;
- un risque entre 10 et 20 % est considéré comme intermédiaire ;
- un risque supérieur à 30 % est un risque majeur.
Lors de l’estimation du risque, il faut prendre en compte le risque coronarien et le risque d’AVC (un tiers du risque coronaire), le poids relatif de ce dernier s’accentuant avec le vieillissement.
III Tabac
A Prévalence du tabagisme en France
Dans la population adulte, 30 % fument régulièrement, 50 % des jeunes de 18 à 24 ans. Chez les femmes enceintes, 25 % continuent à fumer pendant leur grossesse.
B Risque cardiovasculaire et tabac
Parmi les fumeurs ayant débuté à l’adolescence et poursuivant leur intoxication, 50 % mourront du fait de complications directement liées au tabagisme. La relation dose-effet (complications ischémiques) est continue et se manifeste dès la première cigarette quotidienne dans les études épidémiologiques puissantes. Même le tabagisme passif accroît le risque de complication vasculaire ischémique.
La diminution du risque ischémique après sevrage est rapide : abaissement des deux tiers du surcroît de risque à l’issue de la première année et retour quasiment au risque de base après la troisième année de sevrage. Le tabagisme agit surtout par son mécanisme prothrombotique, ce qui explique l’effet nocif précoce et le bénéfice rapide lors du sevrage.
Le tabac prédispose plus particulièrement au risque de maladie coronarienne et d’artériopathie des membres inférieurs :
- RR = 3 de maladie coronarienne chez les fumeurs (> 20 cigarettes par jour) par rapport aux non-fumeurs ;
- RR = 5 d’infarctus du myocarde et de mort subite chez les grands fumeurs inhalant la fumée ;
- RR = 2 à 7 d’AOMI selon les études et l’intensité de la consommation ;
- RR = 1,5 à 2 d’AVC.
La poursuite du tabagisme après l’apparition de la maladie aggrave fortement le pronostic : dans le cas de la maladie coronarienne avérée, le risque de décès ou la nécessité d’une intervention itérative sont multipliés par un facteur 1,5 à 2,5 en cas de tabagisme persistant.
L’association tabagisme et contraception œstroprogestative comporte une nocivité particulière par majoration du risque thromboembolique.
IV Hyperlipidémies
A Rappel succinct sur le métabolisme lipidique
On décrit plusieurs lipoprotéines, qui sont des particules en charge du transport des lipides dans le plasma :
- les chylomicrons, synthétisés dans la cellule intestinale, qui transportent les lipides d’origine alimentaire ;
- les VLDL(Very Low Density Lipoproteins), synthétisées dans le foie, contenant du cholestérol et des triglycérides ; ceux-ci sont hydrolysés dans la circulation en IDL (Intermediate Density Lipoproteins) puis en LDL (Low Density Lipoproteins) ;
- les LDL sont captées au niveau des cellules périphériques et hépatiques par un récepteur spécifique, le LDL-récepteurqui est, entre autres, sous le contrôle de la proprotéine convertase subtilisine/kexine de type 9 (PCSK9) ;
- les HDL (High Density Lipoproteins), produites par le foie, qui jouent un rôle essentiel dans la captation du cholestérol dans les tissus périphériques pour le rapporter au foie en vue de sa dégradation (voie de retour du cholestérol).
Parmi, les enzymes clés du métabolisme lipidique, citons la lipoprotéine lipase, qui est en charge de la dégradation des triglycérides au sein des chylomicrons et des VLDL.
B Relations
La morbi-mortalité cardiovasculaire est associée à :
- une augmentation du LDL-cholestérol (LDLc) ;
- une augmentation des triglycérides(TG) ;
- une diminution du HDL-cholestérol (HDLc).
L’hypertriglycéridémie constitue un facteur de risque cardiovasculaire moins puissant que l’augmentation du LDLc. L’hypertriglycéridémie alliée à un taux de HDL-cholestérol diminué est associée à une augmentation du risque cardiovasculaire (dans le cadre du syndrome métabolique).
La diminution du HDLc est un marqueur de risque indépendant puissant, en revanche des données récentes suggèrent que ce ne serait pas un facteur de risque indépendant. On insiste de plus en plus sur la fonctionnalité des HDL, qui peut être altérée dans certaines situations cliniques (diabète, par exemple). Le dosage du HDLc demeure utile en prédiction cardiovasculaire mais, en revanche, normaliser sa concentration ne constitue plus une cible.
Les facteurs de risque cardiovasculaire favorisent l’athérosclérose, dont les conséquences sont la sténose artérielle ischémique chronique (angor d’effort, claudication intermittente…) et les pathologies vasculaires aiguës par rupture de la plaque d’athérome (syndrome coronaire aigu, AVC ischémique, ischémie aiguë d’un membre inférieur…) (cf. Item 218). La physiopathologie de l’athérosclérose est complexe et ne rentre pas dans le cadre de ce chapitre. En résumé, HTA, tabagisme, diabète et dyslipidémies induisent des dysfonctions endothéliales et le dépôt des lipoprotéines athérogènes (principalement les LDL). Le temps de séjour allongé et l’environnement inflammatoire local provoquent l’oxydation des LDL dans la paroi artérielle, qui ne sont alors plus reconnues par le récepteur LDL-R. L’hypothèse physiopathologique majeure implique le recrutement de macrophages (entre autres types cellulaires) au niveau de la plaque naissante, qui, via des récepteurs de type SR-A, internalisent les LDL oxydées et se transforment en cellules spumeuses (chargées de gouttelettes cytoplasmiques d’esters de cholestérol), marqueur histologique des plaques d’athérome.
C Diagnostic positif d’une hyperlipidémie
1 Signes évocateurs
Hypercholestérolémies
Parfois, des dépôts lipidiques banals sont observés :
- arc cornéen (valeur sémiologique avant 60 ans) ;
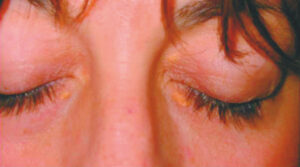
- xanthélasma (valeur sémiologique avant 60 ans) (fig. 3).
________________________________________________________________________________
Fig. 3.
Xanthélasma.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
Plus rarement, des xanthomes sont retrouvés :
- xanthomes tendineux au niveau :
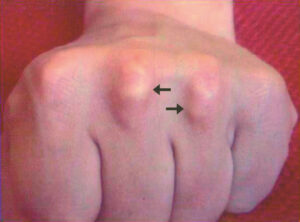
- des extenseurs des doigts (fig.4) ;
________________________________________________________________________________
Fig. 4.
Xanthomes tendineux, extenseurs des doigts.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
-
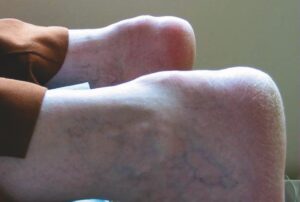
- des tendons calcanéens (fig .5) ;
________________________________________________________________________________
Fig. 5.
Xanthomes achilléens.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
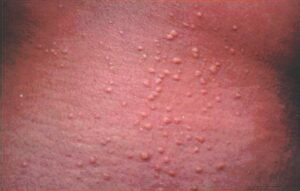
- xanthomes plans cutanés, xanthomes tubéreux (uniquement les formes homozygotes) (fig.6).
________________________________________________________________________________
Fig. 6.
Xanthomes tubéreux.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
Hypertriglycéridémies
Exceptionnellement, un syndrome hyperchylomicronémique peut être observé : hépatomégalie stéatosique, douleurs abdominales, xanthomatose éruptive, lipémie rétinienne (fig. 7).
________________________________________________________________________________
Fig. 7.
Syndrome hyperchylomicronémique.
A. Xanthomatose éruptive. B. Lipémie rétinienne.
(Source : CEEDMM, 2021.)

________________________________________________________________________________
2 Complications des hyperlipidémies
Hypercholestérolémies
Complications athéromateuses parfois révélatrices de l’hyperlipidémie : insuffisance coronaire (infarctus du myocarde), artériopathie des membres inférieurs, AVC.
Hypertriglycéridémies
Rarement, une pancréatite aiguë peut être observée, surtout lors des hyperchylomicronémies. Le risque est majoré selon la triglycéridémie : on considère classiquement que le risque se manifeste pour des triglycérides > 10 g/l. Il dépend principalement des antécédents personnels et de l’intensité maximale des pics de triglycéridémie.
3 Bilan lipidique
Ce bilan est orienté dans le cadre :
- d’une enquête familiale devant une dyslipidémie chez un apparenté ;
- d’une pathologie associée ou d’une prescription induisant une dyslipidémie secondaire ;
- de la présence d’un ou plusieurs facteurs de risque coexistant (estimation du risque cardiovasculaire absolu).
Ses modalités de réalisation sont les suivantes :
- il doit être effectué après 12 heures de jeûne ;
- étant prescrit devant un facteur de risque cardiovasculaire ou une complication, il se doit d’être complet pour mieux stratifier le risque et il doit être répété en cas d’anomalies pour confirmation ;
- si les anomalies lipidiques ne sont pas suffisamment importantes pour justifier un traitement, le bilan lipidique doit alors être contrôlé tous les 3 ans, sauf pour les diabétiques de type 2 chez qui il doit être vérifié annuellement ;
- comme l’âge est un facteur de risque, il est logique que le bilan lipidique soit contrôlé systématiquement vers la cinquantaine chez les hommes et la soixantaine chez les femmes.
L’exploration d’une anomalie lipidique (EAL) comporte :
- une mention de l’aspect du sérum (les hypertriglycéridémies comportent systématiquement un aspect trouble du sérum) ;
- le dosage du cholestérol total, des triglycérideset du HDL-cholestérol (HDLc) ;
- le calcul du LDL-cholestérol (LDLc) par dosage direct ou avec la formule de Friedewald (avec Ct correspondant au cholestérol total) :
- LDLc = Ct – HDLc – TG/5 [g/l] (formule utilisable si TG < 3,4 g/l) ;
- LDLc = Ct – HDLc – TG/2,19 [mmol/l] (formule utilisable si TG < 3,9 mmol/l).
Le calcul du LDL-cholestérol est indispensable pour affirmer le caractère athérogène d’une hyperlipidémie. En cas de triglycérides > 3,4 g/l [3,9 mmol/l], la formule de Friedewald n’est plus valide pour calculer le LDL-cholestérol : il faut alors réaliser un dosage direct du LDL-cholestérol.
D Diagnostic étiologique d’une hyperlipidémie
1 Hyperlipidémies secondaires
Les hyperlipidémies secondaires s’améliorent avec un traitement à visée étiologique, sans employer d’hypolipémiants, ici inutiles voire dangereux dans certaines situations — par exemple, risque d’effet secondaire musculaire sous statine lors de l’hypothyroïdie.
Une hyperlipidémie peut se rencontrer dans les situations suivantes.
Endocrinopathies
Hypothyroïdie
C’est l’une des principales causes d’hyperlipidémie secondaire. Elle est caractérisée par une hypercholestérolémie avec augmentation du LDL-cholestérol et aussi du HDL-cholestérol.
Hypercortisolisme
Il s’accompagne d’une augmentation des triglycérides et d’une diminution du HDL-cholestérol.
Maladies rénales
Insuffisance rénale
Elle s’accompagne d’une augmentation des triglycérides.
Syndrome néphrotique
Il est à l’origine d’une augmentation du cholestérol et des triglycérides.
Atteinte hépatique
Cholestase
Il est observé, lors d’une cholestase, une augmentation du cholestérol qui peut être importante.
Médicaments
Plusieurs médicaments peuvent occasionner des hyperlipidémies :
- la ciclosporine (hypercholestérolémie prépondérante avec interaction médicamenteuse prévisible sous statine) ;
- les corticoïdes (augmentation des triglycérides, effet sur le cholestérol variable) ;
- les œstrogènes par voie orale (éthinyl-œstradiol à dose contraceptive, hypertriglycéridémie avec HDLc conservé) ;
- les rétinoïdes (essentiellement sur un terrain prédisposé à une hyperlipidémie combinée familiale) ;
- l’interféron alpha ;
- certains antirétroviraux : ils peuvent générer des hypertriglycéridémies majeures, le plus souvent chez des malades prédisposés ;
- les neuroleptiques : certains de troisième génération (hypertriglycéridémie prépondérante) ;
- les diurétiques thiazidiques, les bêtabloquants non sélectifs sans activité sympathomimétique intrinsèque (hypertriglycéridémie discrète) ;
- certains traitements anticancéreux : inhibiteurs mTOR qui peuvent entraîner une augmentation du cholestérol (LDL-cholestérol) et des triglycérides.
Bilan minimal d’identification d’une dyslipidémie secondaire
Les examens sont guidés par le contexte et la clinique : TSH, créatininémie, protéinurie, bandelette urinaire ± phosphatases alcalines.
À part, l’hyperlipidémie associée au diabète de type 2 et au syndrome métabolique
Il ne s’agit pas précisément d’une hyperlipidémie secondaire dans la mesure où la dyslipidémie observée au cours du diabète de type 2 ne régresse pas après normalisation de la glycémie. Cette dyslipidémie fréquente est associée à l’état d’insulinorésistance notée au cours du syndrome métabolique et du diabète de type 2.
Le syndrome métabolique, avec ou sans diabète de type 2, est très fréquent, observé dans 10 à 25 % de la population adulte et témoigne d’un état d’insulinorésistance. Son diagnostic est retenu encas de présence d’au moins trois des cinq facteurs suivants (critères NCEP/ATP III) (tableau 1) :
- obésité androïde : périmètre abdominal> 102 cm chez l’homme et > 88 cm chez la femme ;
- triglycérides ≥ 1,5 g/l ;
- HDL-cholestérol bas : < 0,40 g/l chez l’homme, < 0,50 g/l chez la femme ;
- pression artérielle≥ 130/85 mmHg (ou hypertension artérielle traitée) ;
- glycémie à jeun ≥ 1,10 g/l.
Le syndrome métabolique est associé à un risque cardiovasculaire augmenté.
________________________________________________________________________________
Tableau 1.
Définition du syndrome métabolique (critères NCEP III).
Le surpoids et l’obésité sont associés à l’insulinorésistance et au syndrome métabolique ; cependant, l’obésité androïde est mieux corrélée au syndrome que l’indice de masse corporelle (IMC) : la mesure du tour de taille est recommandée pour identifier le syndrome métabolique. (Source : CEEDMM, 2021.)
| Facteur de risque | Niveau seuil |
| Obésité abdominale
– Homme – Femme |
Tour de taille (+++)
> 102 cm > 88 cm |
| Triglycérides | ≥ 1,5 g/l |
| HDL-cholestérol | |
| – Homme
– Femme |
< 0,4 g/l
< 0,5 g/l |
| Pression artérielle | ≥ 130/85 mmHg |
| Glycémie à jeun | ≥ 1,10 g/l |
________________________________________________________________________________
2 Hyperlipoprotéinémies primaires
Les hyperlipidémies primaires sont classifiées en :
- hypercholestérolémies isolées ;
- hypertriglycéridémies isolées ;
- hyperlipidémies mixtes.
Il existe, par ailleurs, une classification historique, la classification de Fredrickson, fondée sur le phénotype lipidique (fig. 8). Les classifications des hyperlipidémies primaires sont présentées sur le tableau 2.
________________________________________________________________________________
Tableau 2.
Classification des hyperlipoprotéinémies. (Source : CEEDMM, 2021.)
| Classification simplifiée | Classification de Fredrickson |
| Hypercholestérolémie pure | Hypercholestérolémie pure familiale (IIa)
Hypercholestérolémie pure polygénique (IIa) |
| Hypertriglycéridémie pure | Hyperchylomicronémie (I)
Hypertriglycéridémie familiale (IV) Hyperlipidémie de type V (I + IV) |
| Hyperlipidémie mixte | Hyperlipidémie familiale combinée (IIb ou IIa ou IV)
Dysbêtalipoprotéinémie (III) |
________________________________________________________________________________
________________________________________________________________________________
Fig. 8.
Phénotypes des plasmas.
- Hyperlipidémie de type IIa : sérum limpide en cas d’hypercholestérolémie pure, quelle que soit son intensité.
- Hypertriglycéridémie pure : hyperlipidémie de type I : couche crémeuse correspondant à une élévation des chylomicrons ; hyperlipidémie de type V : anneau crémeux et sérum de couleur blanchâtre correspondant à une élévation des chylomicrons (I) et des VLDL (IV).
- Hyperlipidémie mixte : exemple d’hyperlipidémie familiale combinée, de type IV ou de type IIb, sérum trouble du fait de l’accumulation de VLDL.
(Source : CEEDMM, 2021.)

________________________________________________________________________________
Il faut savoir que pour plusieurs hyperlipidémies, un même génotype peut, selon le contexte environnemental, correspondre à plusieurs phénotypes lipidiques. Le phénotype lipidique correspond donc à une situation instantanée qui ne permet pas nécessairement de préjuger du mécanisme physiopathologique sous-jacent.
Hypercholestérolémie isolée
Hypercholestérolémie pure familiale (type IIa)
Il s’agit d’une maladie familiale liée à une mutation monogénique. Il peut s’agir d’une mutation :
- du gène du récepteur des LDL (environ 80 %) (mutation inactivatrice à transmission autosomique dominante) ;
- du gène de l’ApoB100 (5 à 10 %) (mutation inactivatrice) ;
- du gène PCSK9(< 5 %) (mutation gain de fonction).
L’hypercholestérolémie familiale peut se présenter sous la forme homozygote ou sous la forme hétérozygote.
Forme homozygote
Cette forme est rare : sa fréquence est de l’ordre d’un cas pour 500 000 (doubles hétérozygotes, homozygotes lorsque consanguinité).
Caractéristiques inhérentes à cette forme :
- LDLc > 4 g/l (6 à 10 g/l) ;
- dépôts lipidiques dès l’enfance : xanthomatose cutanéotendineuse (xanthomes plans, tubéreux et tendineux majeurs) ;
- complications cardiovasculaires ischémiques dès la première décennie ; en l’absence de traitement : décès vers l’âge de 20 ans ;
- fréquence (+++) des rétrécissements aortiques athéromateux supravalvulaires.
Forme hétérozygote
Sous cette forme, 50 % des récepteurs sont fonctionnels ; la prévalence atteint 0,2 % dans la population générale et 3 % parmi les individus ayant un infarctus du myocarde.
Caractéristiques liées à la forme hétérozygote du gène du récepteur des LDL :
- LDLc compris entre 2 et 4,0 g/l (phénotype IIa) ;
- xanthomes tendineux présents dans 30 % des cas seulement ;
- complications cardiovasculaires ischémiques précoces en l’absence d’hypocholestérolémiant efficace :
- chez l’homme : vers 40 à 50 ans ;
- chez la femme : vers 50 à 60 ans.
En cas d’hypercholestérolémie familiale, il sera important de faire un dépistage d’une hypercholestérolémie chez les apparentés au premier degré.
Hypercholestérolémies polygéniques (type IIa)
Caractéristiques de ces hypercholestérolémies :
- absence d’hérédité familiale mendélienne ;
- physiopathologie inconnue ;
- fréquence élevée : elle représente la majorité des hypercholestérolémies modérées ;
- facteurs favorisants ou aggravants, tels que les erreurs de régime (riche en cholestérol et en graisses saturées) ;
- complications cardiovasculaires plus tardives que dans l’hypercholestérolémie familiale, puisque l’installation de l’hypercholestérolémie est survenue seulement vers la quarantaine.
Hypertriglycéridémie isolée
Hyperchylomicronémies primitives familiales
Les formes avec hyperchylomicronémie exclusive (type I) sont exceptionnelles. Cette hyperchylomicronémie est secondaire à une anomalie génétique responsable d’un déficit d’activité de la lipoprotéine lipase (enzyme responsable de la dégradation des chylomicrons et des VLDL).
Hypertriglycéridémie familiale
Les caractéristiques de ce type d’hyperlipidémie sont les suivantes :
- fréquence rare ;
- transmission autosomique dominante ;
- accumulation de VLDL endogène (type IV) ;
- dépendance au surpoids ;
- pas de xanthomes ;
- risque de décompensation sur un mode de syndrome hyperchylomicronémique (type V = type I [chylomicrons] + type IV [VLDL]) ;
- caractère athérogène débattu.
Hyperlipidémies combinées familiales
Ce sont les dyslipidémies les plus fréquentes : 1 à 2 % de la population générale ; elles affectent 10 % des sujets présentant un infarctus avant 60 ans.
Caractéristiques de ces hyperlipidémies :
- transmission héréditaire non mendélienne oligogénique ;
- jamais de xanthomes ;
- intrication avec un syndrome métabolique ;
- révélation tardive à l’âge adulte mais d’autant plus précocement qu’il existe une obésité ;
- phénotypes lipidiques variables dans la même famille et fluctuant chez un même individu au fil du temps, type IIb principalement (augmentation du LDLc et des triglycérides) mais aussi type IIa (augmentation isolée du LDLc) ou type IV (augmentation isolée des triglycérides) ;
- derrière cette hétérogénéité phénotypique, un trait commun des hyperlipidémies combinées est l’augmentation d’une sous-classe particulière de LDL, dites LDL petites et denses (small dense LDL) ; leur synthèse est favorisée par l’hypertriglycéridémie et leur pouvoir athérogène est élevé ; les LDL petites et denses sont retrouvées également dans le syndrome métabolique et le diabète de type 2 et rendraient compte, pour partie, de l’augmentation du risque cardiovasculaire associé à ces deux pathologies ; l’analyse des sous-classes de LDL n’est toutefois pas encore possible en pratique courante ;
- complications cardiovasculaires fonction de l’intensité de la dyslipidémie.
Les différents phénotypes lipidiques peuvent être rencontrés chez un même sujet au fil du temps et, simultanément, chez au moins un apparenté au premier degré.
Dysbêtalipoprotéinémie (type III)
Hyperlipidémie combinée rare, caractérisée par une élévation harmonieuse de la cholestérolémie et de la triglycéridémie.
V Hypertension artérielle et risque cardiovasculaire
A Définition
________________________________________________________________________________
Pression artérielle systolique ≥ 140 mmHg et/ou pression artérielle diastolique ≥ 90 mmHg, confirmée au minimum par deux mesures lors de trois consultations successives sur une période de 3 à 6 mois.
________________________________________________________________________________
Les techniques de mesure sont d’une part l’automesure tensionnelle et, d’autre part, la MAPA (mesure automatisée de la pression artérielle). Sa valeur pronostique apparaît supérieure à celle de la mesure effectuée au cabinet médical. Elle permet de s’affranchir de l’HTA « blouse blanche ». Les seuils sont décalés :
- de 5 mmHg en automesures isolées : 135/85 mmHg ;
- de 10 mmHg en MAPA moyennée sur 24 heures : 130/80 mmHg.
B Prévalence et risque cardiovasculaire
L’HTA affecte 40 % de la population adulte. Sa probabilité de survenue est d’autant plus élevée qu’il existe un syndrome métabolique sous-jacent (cf. tableau 2).
Le lien entre niveau tensionnel et risque cardiovasculaire est continu : il n’y a pas de seuil individualisé en dessous duquel le risque peut être considéré comme nul. La relation entre pression artérielle et risque cérébral est beaucoup plus étroite que la relation entre pression artérielle et risque coronarien. À niveau tensionnel égal, l’HTA est grevée d’un pronostic d’autant plus péjoratif qu’elle s’associe à :
- une hypertrophie ventriculaire gauche(électrique, échographique) ;
- une glomérulopathie, attestée par une élévation de la microalbuminurieavant le stade de l’IRC.
C Bilan diagnostique étiologique et évolutif face à une HTA
(Cf. Item 221 – Hypertension artérielle de l’adulte.)
- Un examen clinique, avec recherche de facteurs provoquant ou aggravant une HTA.
- Un bilan biologique comportant ionogramme sanguin, créatininémie avec débit de filtration glomérulaire estimé, glycémie à jeun, bilan lipidique et protéinurie — la recherche de la microalbuminurie n’est recommandée que chez le sujet diabétique.
- Un électrocardiogramme de repos.
VI Diabète et risque cardiovasculaire
Le risque relatif de complications coronariennes ischémiques est plus élevé chez la femme (RR = 3–4) que chez l’homme (RR = 2–3).
Le risque relatif d’AOMI (avec des formes généralement infrapoplitées) est particulièrement élevé lors du diabète : RR = 5.
L’augmentation du risque relatif d’AVC (RR = 2–3) correspond en grande partie à une fréquence accrue de lacunes (atteintes des petites artères perforantes) en lien étroit avec l’HTA.
Dans le diabète de type 1, le risque n’apparaît qu’après 15 à 20 ans d’évolution et essentiellement lorsqu’il existe une atteinte rénale concomitante avec protéinurie.
Dans le diabète de type 2, la maladie coronarienne peut précéder fréquemment l’émergence du diabète proprement dit, du fait du long passé de syndrome métabolique.
L’ancienneté du diabète favorise la survenue de manifestations coronariennes ischémiques, dont cliniquement silencieuses. Puisque l’insuffisance coronarienne est plus souvent silencieuse chez les sujets diabétiques (risque relatif de coronaropathie sans douleur typique 2 fois plus élevé), les sujets diabétiques à très haut risque cardiovasculaire sont soumis à des tests de dépistage (+++). Ce dépistage n’est pas systématique car il n’a pas été établi qu’il débouchait sur un bénéfice cardiovasculaire mais réalisé seulement chez les malades ayant une très forte probabilité de lésion coronaire.
L’intensité du risque demeure fonction du nombre de facteurs de risque surajoutés, de leur ancienneté et de leur intensité. Ainsi, le niveau de risque cardiovasculaire est moins prononcé s’il n’y a pas de syndrome métabolique associé. La survenue d’une néphropathie avérée avec IRC évoluée ou protéinurie correspond à un risque cardiovasculaire élevé.
Il n’existe pas de valeur seuil de la glycémie conditionnant le risque de complications macrovasculaires. L’hyperglycémie en elle-même est un facteur de risque cardiovasculaire de complication macrovasculaire bien moins puissant que pour le risque de complication microvasculaire. Il est établi qu’un contrôle glycémique strict permet de réduire le risque cardiovasculaire dans le diabète de type 1 ; la preuve est moins formelle dans le diabète de type 2. En revanche, l’HTA majore puissamment le risque d’AVC.
VII Prise en charge du risque cardiovasculaire
A Principes généraux
1 Concepts
On ne traite pas un bilan lipidique ou des mesures manométriques mais une personne ayant un risque de complication ischémique.
L’efficience du traitement est donc fonction du niveau de risque absolu de chaque individu. Une maladie métabolique chronique implique un traitement chronique, d’autant plus que le risque cardiovasculaire s’accroît en vieillissant.
La découverte d’une pathologie métabolique majorant le risque cardiovasculaire, telle que le diabète ou une dyslipidémie, justifie un dépistage familial (+++).
La mise en route d’un traitement de prévention cardiovasculaire au long cours doit comporter un temps d’information permettant une prise de conscience des enjeux, de la rentabilité du traitement et de la balance bénéfices/risques.
En situation de risque intermédiaire et d’hésitation sur la mise en route d’un traitement au long cours, il peut être utile de s’appuyer alors sur une recherche d’athérome infraclinique prématuré.
Certains médicaments sont pourvoyeurs d’effets secondaires dont certains potentiellement dangereux (par exemple, un risque hémorragique sous antiagrégants) ; le ratio bénéfice/risque et le coût doivent être pris en compte et pas seulement le bénéfice potentiel.
2 Stratégie
Les mesures diététiques sont systématiques en prévention secondaire et primaire.
L’obtention d’un sevrage du tabac est une mesure majeure.
La mise en œuvre des mesures non médicamenteuses ne doit pas retarder l’initiation d’un traitement pharmacologique chez les patients dont le risque cardiovasculaire est élevé.
L’efficacité, la tolérance et l’observance des traitements doivent être surveillées. Le rapport risque/bénéfice doit être réévalué au décours de l’évolution au long cours du malade.
B Sevrage du tabac
En dehors d’épisodes de dépression caractérisée, lors desquels le sevrage du tabac ne doit être envisagé qu’après stabilisation de l’état neuropsychique, le conseil minimal d’aide à l’arrêt du tabac s’adresse à tous les patients. La dépendance à la nicotine doit être évaluée lors d’un projet de sevrage ; une aide au sevrage par substituts nicotiniques est recommandée.
C Activité physique
L’activité physique exerce des effets métaboliques sur :
- le développement de la masse musculaire et la réduction de la masse grasse, induisant :
- une réduction de l’insulinorésistance ;
- une diminution particulière de la triglycéridémie et une augmentation du HDLc ;
- le système cardiovasculaire avec :
- une diminution de la pression artérielle au repos ;
- un allongement du périmètre de marche pour les AOMI ;
- un meilleur pronostic des complications coronariennes ischémiques, probablement via des mécanismes de préconditionnement.
Sa préconisation est systématiquement associée aux mesures diététiques car elle potentialise l’efficacité de ces dernières.
La prescription doit être adaptée à chaque individu et à ses capacités : en cas de très haut risque, il est prudent de vérifier auparavant l’épreuve d’effort.
Il faut préconiser, dans la mesure du possible, une activité régulière sous forme de trois séances hebdomadaires de 30 à 45 minutes, à 75 % de la VO2 maximale (consommation d’oxygène). Si cet optimum ne peut être obtenu, une activité physique moindre est néanmoins justifiée.
D Diététique
1 Mesures lipidiques globales
La liste des mesures préconisées est la suivante :
- avoir un apport quotidien en graisses alimentaires < 35 % de l’apport calorique total ;
- réduire les acides gras saturés (≤ 8–10 %) et maintenir les apports d’acide gras trans aussi bas que possible ;
- privilégier l’apport des graisses mono-insaturées (15 %) ;
- encourager la consommation d’acides gras n–3 à longues chaînes (poissons gras, noix, aliments enrichis en oméga 3) ;
- limiter la dose quotidienne de cholestérol (< 300 mg par jour) ;
- la consommation de fruits et légumes sera encouragée (en raison de leur effet antioxydant).
2 Mesures non lipidiques
Ces mesures, qui portent également sur l’HTA, sont les suivantes :
- favoriser l’apport de fruits et légumes (riches en antioxydants et en fibres) ;
- la consommation régulière de noix, noisettes, amandes a montré un bénéfice cardiovasculaire lors d’un essai d’intervention randomisé ;
- modérer l’apport sodé (< 6 à 8 g par jour) : éviter les excès de charcuterie, conserves, plats préparés, poissons fumés, fruits de mer ; ne pas resaler les plats ;
- limiter la consommation d’alcool à moins de trois équivalents verres de vin par jour et ne pas la proscrire sauf en cas de dépendance ;
- modérer les apports en sucres simples, en particulier le fructose ;
- encourager une réduction pondérale, même limitée, en réduisant l’apport calorique de 20 % en cas de surpoids ou de syndrome métabolique.
3 Mesures diététiques propres aux hypertriglycéridémies
Hypertriglycéridémies modérées
Insister sur la réduction du surpoids, avec apports caloriques équilibrés modérément hypocaloriques (– 20 %) (+++) et la majoration concomitante de l’activité physique.
Procéder à un test d’éviction de l’alcool et des sucres simples, selon la règle suivante :
- suspension de la consommation d’alcool pendant une semaine ;
- réduction des apports glucidiques :
- < 45 % du total calorique ;
- en particulier des sucres simples (fructose et monosaccharide particulièrement hypertriglycéridémiants).
Hypertriglycéridémies majeures (hyperchylomicronémies)
Dans ces formes rares, une prise en charge par une équipe spécialisée est recommandée. En complément des mesures diététiques habituelles des hypertriglycéridémies (cf. supra), on mettra en place un régime hypolipidique à moins de 20 g de graisses par jour. On pourra utiliser des huiles constituées de triglycérides à chaîne moyennes (absorbées directement, sans passer par la voie des chylomicrons).
En situation de décompensation avec une triglycéridémie à plus de 30 g/l, il s’agit d’une urgence nutritionnelle avec mise en place d’une diète hydrique transitoire jusqu’à normalisation ou stabilisation de la triglycéridémie.
E Médicaments hypolipidémiants
Les différentes classes de ces médicaments et leurs principales caractéristiques sont présentées dans le tableau 3, ainsi que leurs mécanismes d’action, leur efficacité, leurs indications, les effets indésirables et les contre-indications.
________________________________________________________________________________
Tableau 3.
Médicaments hypolipidémiants (sauf les anti-PCSK9).
PPAR, Peroxysome Proliferator-Activated Receptor ; AGL, acides gras libres ; Lp(a), lipoprotéine (a) ; CPK, créatine phosphokinase. (Source : CEEDMM, 2021.)

________________________________________________________________________________
Les interactions médicamenteuses, les associations possibles avec les autres agents hypolipidémiants et le niveau de preuve de leur efficacité cardiovasculaire sont indiqués pour chaque classe d’agent hypocholestérolémiant sur le tableau 4 (sauf les anti-PCSK9, encadré).
________________________________________________________________________________
Tableau 4.
Médicaments hypocholestérolémiants (sauf les anti-PCSK9) : interactions médicamenteuses, associations possibles avec les autres agents hypolipidémiants et niveau de preuve cardiovasculaire.
CYP3A4, cytochrome P450 3A4. (Source : CEEDMM, 2021.)

________________________________________________________________________________
________________________________________________________________________________
Encadré – Inhibiteurs de la PCSK9
La PCSK9 est la proprotéine convertase subtilisine/kexine de type 9. Ses inhibiteurs sont de nouveaux agents hypocholestérolémiants puissants. Ils réduisent le taux de LDL-cholestérol de 60 % ou plus. Ils réduisent par ailleurs le taux plasmatique de Lp(a).
Les deux molécules disponibles en France sont l’alirocumab (Praluent®) et l’évolocumab (Repatha®).
Ce sont des traitements injectables (par voie sous-cutanée) administrés toutes les 2 semaines.
Indications limitées :
- aux formes d’hypercholestérolémies très sévères : hypercholestérolémie familiale homozygote, hypercholestérolémies familiales pour lesquelles une LDL-aphérèseest indiquée — LDL-aphérèse : technique d’épuration sanguine extracorporelle permettant d’extraire le LDL-cholestérol ;
- aux patients ayant une maladie cardiovasculaire athéroscléreuse établie par un antécédent de syndrome coronarien aigu récent (prévention secondaire) et qui ne sont pas contrôlés (LDL-cholestérol ≥ 0,70 g/l) malgré un traitement hypolipémiant optimisé comprenant au moins une statine à la dose maximale tolérée (traitement à associer à ce traitement optimisé).
Traitement commencé seulement par un spécialiste (endocrinologue, médecine interne, cardiologue).
________________________________________________________________________________
F Principes du traitement médicamenteux des hypercholestérolémies isolées
1 Introduction du traitement
- En prévention primaire, si le LDL-cholestérol reste élevé (au-dessus de l’objectif) après 3 à 6 mois au minimum de diététique bien conduite.
- En prévention secondaire, avec prise médicamenteuse d’emblée, après une complication ischémique ou en cas de risque équivalent.
2 Objectifs lipidiques
Les objectifs thérapeutiques pour la population générale, en termes de LDL-cholestérol, dépendent du profil de risque cardiovasculaire du patient. L’estimation du niveau de risque cardiovasculaire sera faite, idéalement, à l’aide des équations européennes SCORE 2 (Systematic COronary Risk Evaluation), évaluant le risque de survenue d’un accident cardiovasculaire à 10 ans, chez les sujets de 40 à 69 ans, et SCORE-OP (SCORE-Old People), évaluant le même risque chez les sujets de plus de 70 ans (Consensus Européen ESC 2021). Ces équations sont basées sur la concentration sérique de cholestérol non-HDL, le tabagisme, la pression artérielle systolique, l’âge et le sexe.
Ces équations ne seront pas utilisées dans les situations suivantes :
- Diabète (type 1 ou type 2)
- Hypercholestérolémie familiale
- Insuffisance rénale
En cas de non utilisation des équations SCORE2 ou SCORE-OP, le niveau de risque peut, éventuellement, être apprécié à l’aides des facteurs de risque traditionnels (consensus SFE-SFD-NSFA, 2016) (tableau 5). Les différents niveaux de risque cardiovasculaire et leurs critères sont présentés sur le tableau 6.
________________________________________________________________________________
Tableau 5.
Facteurs de risque cardiovasculaire principaux à considérer lorsque les équations SCORE2 et SCORE-OP ne sont pas utilisables (consensus SFE-SFD-NSFA, 2016).
(Source : CEEDMM, 2021.)
| Âge (≥ 50 ans chez l’homme, ≥ 60 ans chez la femme) |
| Antécédents familiaux d’accident cardiovasculaire ischémique (≤ 55 ans chez le père ou un parent du premier degré, ≤ 60 ans chez la mère ou une parente du premier degré) |
| Tabagisme (actuel ou arrêté depuis moins de 3 ans) |
| Hypertension artérielle |
| HDLc ≤ 0,4 g/l [≤ 1,0 mmol/l] |
________________________________________________________________________________
________________________________________________________________________________
Tableau 6.
Niveaux de risque cardiovasculaire.
% SCORE = risque de décès cardiovasculaire en 10 ans selon la table SCORE2 (cf. fig. 2) ; CV, cardiovasculaire ; FRCV, facteur de risque cardiovasculaire. (Source : CEEDMM, 2021.)
| Niveau de risque cardiovasculaire | |
| Faible | – 0 % ≤ SCORE2 < 1 %
– Ou : 0–1 FRCV |
| Intermédiaire | – 1 % ≤ SCORE2 < 5 %
– Ou : 2 FRCV |
| Élevé | – 5 % ≤ SCORE2 < 10 %
– Ou : ≥ 3 FRCV |
| Très élevé | – SCORE2 ≥ 10 %
– Prévention secondaire |
________________________________________________________________________________
Evaluation du risque cardiovasculaire dans les situations particulières :
- Diabète de type 2 ou de type 1 (consensus SFD/SFC 2021) :
- Risque très élevé : Au moins 1 critère suivant :
- ATCD CV (y compris FA)
- LDL >1,90 g/l sous traitement
- Albuminurie> 300 mg/24h
- DFG < 30 ml/mn
- ECG: ondes Q
- Echo: anomalies VG
- Sténose artère périphérique ≥50%
- Risque élevé : Au moins 2 critères suivants:
- Durée diabète ≥ 10 ans (DT2), ≥ 20 ans (DT1)
- ATCD familiaux de maladie coronarienne (H<50 ans, F< 60 ans)
- FRCV non contrôlés (HbA1c, LDLc, TA, Tabac)
- Microalbuminurie.ou DFG < 60 ml/mn
- Rétinopathie sévère ou neuropathie végétative ou dysfonction érectile
- Faible activité physique
- Risque modéré : toutes les autres situations
- Risque très élevé : Au moins 1 critère suivant :
- Insuffisance rénale
- Risque modéré : DFG ≥ 60 et albuminurie < 300 mg/j
- Risque très élevé : DFG < 30 ou 30≤ DFG ≤ 45 et albuminurie > 30 mg/j
- Risque élevé : les autres
- Hypercholestérolémie familiale = d’emblée à risque élevé
3 Traitement de l’hypercholestérolémie
Décision d’un traitement prise selon le taux de LDL-cholestérol en fonction du profil de risque cardiovasculaire du patient
- chez le sujet de plus de 40 ans non atteint de diabète, d’hypercholestérolémie familiale ou d’insuffisance rénale 3
- en cas de risque cardiovasculaire très élevé, un objectif de LDL-cholestérol< 0,55 g/l (1,4 mmol/l) est conseillé (Consensus Européen ESC 2019 : European Heart Journal [2020]) 41, 111-188)
- en cas de risque cardiovasculaire élevé, un objectif de LDL-cholestérol< 0,70 g/l (1,8 mmol/l) est conseillé (Consensus Européen ESC 2019)
- en cas de risque cardiovasculaire intermédiaire, un objectif de LDL-cholestérol< 1,00 g/l (2,6 mmol/l) est conseillé (Consensus Européen ESC 2019)
- en cas de risque cardiovasculaire faible, l’objectif de LDL-cholestérol est moins clair. Si les recommandations européennes (ESC 2019) indiquent qu’il « est possible d’envisager » un objectif de LDL-cholestérol< 1.16 g /l (3, 0 mmol/l), les recommandations de la NSFA-SFD-SFE 2016 fixent une valeur < 1,90 g/l (4,9 mmol/l).
- chez le patient atteint d’’hypercholestérolémie familiale : la situation est différente : en effet, le risque cardiovasculaire élevé de cette pathologie et la précocité de l’hypercholestérolémie justifient un traitement plus précoce. L’objectif idéal se situe à :
- LDLc < 1,35 g/l (3,5 mmol/l) chez les enfants ;(souvent 1.6 g/l jusqu’à la puberté)
- LDLc < 1,0 g/l (2,60 mmol/l) chez les adultes traités précocement sans facteurs de risque cardiovasculaire additionnels (certains praticiens ciblent 1.3 g/l qui est la concentration médiane de la population française)
- LDLc < 0,70 g/l (1,8 mmol/l) chez les adultes traités tardivement avec cumul de facteurs de risque cardiovasculaire additionnels ;
- LDLc < 0,55 g/l (1,4 mmol/l), en prévention secondaire (niveau de preuve limité dans l’Hypercholestérolémie Familiale hétérozygote).
- chez le patient diabétique (consensus SFD/SFC 2021 : Diabetes Metab. 202; 47(2):101185) :
- en cas de risque cardiovasculaire très élevé, un objectif de LDL-cholestérol< 0,55 g/l (1,4 mmol/l) est conseillé
- en cas de risque cardiovasculaire élevé, un objectif de LDL-cholestérol< 0,70 g/l (1,8 mmol/l) est conseillé
- en cas de risque cardiovasculaire intermédiaire, un objectif de LDL-cholestérol< 1,00 g/l (2,6 mmol/l) est conseillé
- chez le patient insuffisant rénal (recommandations ESC 2019) :
- en cas de risque cardiovasculaire très élevé, un objectif de LDL-cholestérol< 0,55 g/l (1,4 mmol/l) est conseillé
- en cas de risque cardiovasculaire élevé, un objectif de LDL-cholestérol< 0,70 g/l (1,8 mmol/l) est conseillé
4 Traitement médicamenteux
- On commencera un traitement par statine, en première intention.
- Le choix de la statine sera fait en fonction du taux de LDLc initial et de l’objectif visé. L’intensité des différentes statines est reportée sur le tableau 7.
- Si l’objectif est non atteint sous statines à dose maximale, associer de l’ézétimibe voire de la colestyramine.
- En cas d’intolérance aux statines : utiliser l’ézétimibe voire la colestyramine.
- Anti-PCSK9 : dans les hypercholestérolémies familiales sévères (avis spécialisé).
________________________________________________________________________________
Tableau 7.
Intensité des différentes statines. (Source : CEEDMM, 2021.)
| Intensité faible | Intensité modérée | Intensité élevée |
| ↓ LDLc < 30 % | 30 % < ↓ LDLc < 50 % | ↓ LDLc > 50 % |
| – Fluvastatine 20–40 mg
– Pravastatine 10–20 mg – Simvastatine 10 mg |
– Atorvastatine 10–20 mg
– Fluvastatine 80 mg – Pravastatine 40 mg – Simvastatine 20–40 mg – Rosuvastatine 5–10 mg |
– Atorvastatine 40–80 mg
– Rosuvastatine 20 mg |
________________________________________________________________________________
G Principes du traitement médicamenteux des hypertriglycéridémies et des hyperlipidémies mixtes
1 Hypertriglycéridémie isolée (fig. 9)
- Valeur de triglycérides considérée comme normale : < 1,5 g/l [1,7 mmol/l].
- Importance des mesures diététiques : limiter aliments et boissons sucrés ; limiter ou arrêter l’alcool ; consommation de poissons gras riches en oméga 3.
- En cas d’hypertriglycéridémie sévère (> 5 g/l [5,6 mmol/l]) :
- l’objectif est de réduire les triglycérides < 5 g/l pour réduire le risque de pancréatite ;
- commencer un traitement par fibrate ;
- si le taux de triglycérides reste élevé sous fibrates, on pourra y associer des acides gras oméga 3.
________________________________________________________________________________
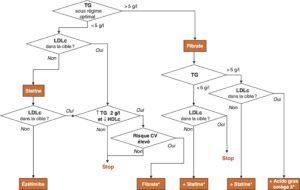
Fig. 9.
Algorithme de prise en charge des hypertriglycéridémies et hyperlipidémies mixtes.
* Sur avis spécialisé.
(Source : CEEDMM, 2021, d’après le consensus SFE-SFD-NSFA, 2016.)
________________________________________________________________________________
2 Hyperlipidémie mixte (fig. 9)
- Dans la dyslipémie mixte l’objectif sur le LDLc reste prioritaire (dans la mesure où les triglycérides sont en règle < 5 g/l [5,6 mmol/l]).
- On aura donc recours aux statines pour atteindre l’objectif de LDL-cholestérol (éventuellement statines + ézétimibe si nécessaire).
- Une fois l’objectif de LDL-cholestérol atteint, il pourra être proposé d’ajouter un traitement par fibrate (fénofibrate préférentiellement ; jamais par le gemfibrozil) chez les patients à haut risque cardiovasculaire dont le taux de triglycérides et supérieur ou égal à 2,0 g/l et dont le HDL-cholestérol est bas (< 0,40 g/l chez l’homme, < 0,50 g/l chez la femme) (fig.9).
Principes d’adaptation du traitement
L’habitude est de commencer les hypolipémiants à faible posologie et de l’augmenter ultérieurement en fonction de l’efficacité et de la tolérance, jusqu’à l’obtention d’un taux de LDL inférieur à la valeur cible.
L’utilisation de fortes doses voire d’une association d’hypolipémiants est à envisager au cas par cas, après avis spécialisé, en veillant à la tolérance et à l’observance du traitement.
Surveillance de l’efficacité du traitement hypolipidémiant
- Pratiquer un bilan lipidique 2 à 3 mois après la mise en route du traitement afin de vérifier que les objectifs lipidiques sont atteints puis annuellement.
- Informer le patient de ces objectifs.
- Si les objectifs thérapeutiques sont atteints, le bilan lipidique est réalisé 1 à 2 fois par an.
- Si les objectifs thérapeutiques ne sont pas atteints, modification de la thérapeutique et bilan lipidique de contrôle 2 mois plus tard, jusqu’à l’obtention des objectifs thérapeutiques.
Surveillance de la tolérance du traitement hypolipidémiant
- Tolérance clinique : douleurs musculaires en particulier.
- Tolérance biologique :
- dosage des transaminases, avant, dans les 3 mois qui suivent l’instauration du traitement et une dernière fois après 1 an ;
- dosage des CPK, seulement en cas de myalgies et/ou de situation à risque majoré (associations médicamenteuses, comorbidités, antécédent d’intolérance).
H Médicaments antihypertenseurs
La HAS a publié un algorithme de prise en charge de l’hypertension artérielle essentielle de l’adulte (hors grossesse) en 2016 (fig. 10) ; pour le détail de la stratégie thérapeutique et le choix des traitements hypertenseurs, nous renvoyons l’étudiant à l’Item 221 traité dans l’ouvrage du Collège national des enseignants de cardiologie et de la Société française de cardiologie (CNEC-SFC) dans la même collection.
________________________________________________________________________________
Fig. 10.
Prise en charge de l’hypertension artérielle de l’adulte, hors grossesse.
AMT, automesure tensionnelle ; MAPA, mesure ambulatoire de la pression artérielle ; ARA II, antagonistes des récepteurs de l’angiotensine II ; IEC, inhibiteurs de l’enzyme de conversion.
Nous remercions la Haute Autorité de santé de nous avoir autorisés à reproduire ces extraits. Il est également consultable sur le site www.has-sante.fr rubrique Toutes nos publications

________________________________________________________________________________
I Antiagrégants plaquettaires
1 Prévention secondaire
Indication systématique, sauf contre-indications absolues.
L’association clopidogrel-aspirine doit être systématique pendant le mois suivant la mise en place d’un stent et pendant l’année suivant l’implantation d’un stent actif. Il existe un risque important d’accident thrombotique dans les 10 jours suivant la suspension de la double association. L’association aspirine-clopidogrel ne doit pas être interrompue sans concertation multidisciplinaire préalable.
L’association aspirine-clopidogrel n’a pas montré de supériorité par rapport au clopidogrel seul en prévention secondaire des accidents vasculaires cérébraux.
Le prasugrel et le ticagrelor ont montré une supériorité face au clopidogrel lors des syndromes coronariens aigus.
2 Prévention primaire
Chez le diabétique ou chez l’hypertendu, l’utilisation systématique des antiagrégants en prévention primaire est l’objet de controverses. Le rapport risque/bénéfice de l’aspirine à faible dose n’a pas été formellement établi dans ces situations.
Par rapport à l’aspirine, le clopidogrel comporte une moindre toxicité gastrique et un risque hémorragique similaire.
J Prise en charge du risque cardiovasculaire lors du diabète
Cf. Item 245 – Diabète sucré de type 1 et 2 de l’enfant et de l’adulte.
________________________________________________________________________________
Points-clés
- Les principaux facteurs de risque modifiables sont le tabagisme, le LDLc élevé, l’hypertension artérielle et le diabète, auxquels on peut rajouter le HDLc bas (marqueur de risque).
- Le risque global peut être calculé par des équations de risque, comme celles de Framingham ou SCORE. Dans les recommandations, l’évaluation du risque se fait toutefois par le décompte des facteurs de risque.
- La relation entre tabac et risque cardiovasculaire est continue et existe aussi dans le tabagisme passif. Le risque est majoré en association à la contraception œstroprogestative.
- La démarche diagnostique dans l’hyperlipidémie, l’hypertension artérielle et le diabète comprend plusieurs étapes : le diagnostic positif (exploration d’une anomalie lipidique dans les dyslipidémies, valeur de l’automesure tensionnelle dans l’hypertension artérielle), le diagnostic des formes secondaires (savoir les identifier) et l’identification du risque du patient. Cette identification conditionne la thérapeutique.
- La prise en charge du risque vasculaire comprend le sevrage tabagique (les patchs à la nicotine peuvent être utilisés en prévention secondaire), les conseils d’activité physique, les mesures diététiques et le traitement adapté de chaque facteur de risque.
- Dans les hyperLDLémies, le traitement de première intention est une statine. Les cibles de LDLc ne sont pas définies avec certitude en dessous de 1 g/l de LDLc. Dans le diabète de type 2, le traitement de choix pour débuter est la metformine. Dans l’hypertension artérielle, une des cinq classes d’antihypertenseurs peut être utilisée en première intention sauf cas particulier (par exemple, en post-infarctus : utilisation des bêtabloquants) ; en bithérapie de l’hypertension artérielle, il faut associer un médicament du groupe bêtabloquant/ARA II/IEC avec un des médicaments du groupe diurétiques thiazidiques/inhibiteur calcique.
________________________________________________________________________________
© CEEDMM – Août 2022.
