Item 308 – Tumeurs neuroendocrines du pancréas
________________________________________________________________________
Situations de départ
- 21 Asthénie.
- 24 Bouffées de chaleur.
- 25 Hypersudation.
- 50 Malaise/perte de connaissance.
- 57 Prise de poids.
- 118 Céphalée.
- 138 Anomalie de la vision.
- 143 Diplopie.
- 165 Palpitations.
- 209 Hypoglycémie.
- 279 Consultation de suivi d’une pathologie chronique.
- 328 Annonce d’une maladie chronique.
- 352 Expliquer un traitement au patient (adulte, enfant, adolescent).
________________________________________________________________________________
________________________________________________________________________________
Hiérarchisation des connaissances
________________________________________________________________________________
| Rang | Rubrique | Intitulé | Descriptif |
| A | Définition | Connaître les deux principaux types histologiques des tumeurs du pancréas | Adénocarcinome, tumeur neuroendocrine |
| B | Prévalence, épidémiologie | Épidémiologie et facteurs de risque de l’adénocarcinome du pancréas et des tumeurs neuroendocrines | Comprenant l’indication de la consultation d’oncogénétique |
| A | Diagnostic positif | Connaître les principaux signes cliniques de l’adénocarcinome du pancréas et des tumeurs neuroendocrines | |
| A | Examens complémentaires | Connaître les indications des examens de biologie devant une tumeur du pancréas | Si douleurs abdominales ou ictère : échographie abdominale transpariétale en première intention, la découverte de la dilatation des voies biliaires amène alors à la réalisation d’un scanner abdominal. Lorsqu’une tumeur est fortement suspectée (ictère nu avec altération de l’état général), c’est le scanner thoraco-abdomino-pelvien qui est l’examen de 1re intention. En cas de doute ou de lésion isodense au scanner, l’IRM permet parfois d’obtenir une meilleure visibilité de la tumeur. Si un doute diagnostique persiste ou si une chirurgie n’est pas indiquée en 1re intention, l’écho-endoscopie permet de voir la tumeur et d’en faire des biopsies pour confirmation histologique |
| B | Examens complémentaires | Connaître les indications des examens d’imagerie d’une tumeur du pancréas | Recherche un cancer du pancréas et fait le bilan d’extension local (envahissement tumoral des axes vasculaires péri-pancréatiques) et à distance (essentiellement sous forme de métastases hépatiques ou d’une carcinose péritonéale) avant tout geste endoscopique, bilan d’opérabilité. Avant toute décision de résection chirurgicale, une IRM hépatique avec imagerie de diffusion est recommandée pour éliminer des métastases hépatiques occultes |
| B | Prévalence, épidémiologie | Épidémiologie descriptive d’une tumeur kystique du pancréas
|
|
________________________________________________________________________________
Tumeurs neuroendocrines du pancréas
- Définitions
- Grades histopronostiques
- Présentation clinique
- Imagerie conventionnelle et fonctionnelle
I Définitions
Les tumeurs neuroendocrines duodénopancréatiques (TNE-DP) sont des tumeurs rares développées aux dépens des cellules endocrines du pancréas et du duodénum.
Le diagnostic est histologique (aspect lobulaire ou trabéculaire dans les formes bien différenciées), mais nécessite une confirmation immunohistochimique (expression de la synaptophysine et la chromogranine A).
II Grades histopronostiques
Le stade tumoral et la classification anatomopathologique OMS 2017 des TNE-DP avec le Ki-67, reflet de l’activité mitotique (tableau 1, fig. 1), sont les deux principaux facteurs pronostiques. Il faut séparer les TNE (bien différenciées), qui sont les plus nombreuses et sont associées à une survie prolongée même en l’absence de traitement, des carcinomes neuroendocrines (peu différenciés) dont le pronostic est très sombre.
________________________________________________________________________________
Tableau 1.
Classification anatomopathologique OMS 2017 des néoplasmes neuroendocrines pancréatiques. (Source : CEEDMM, 2021.)
| Morphologie
(différenciation) |
Grade
(% Ki-67) |
|
| Tumeur neuroendocrine de grade 1
(TNE G1) |
Bien différenciée | G1 (< 3 %) |
| Tumeur neuroendocrine de grade 2
(TNE G2) |
Bien différenciée | G2 (3–20 %) |
| Tumeur neuroendocrine de grade 3
(TNE G3) |
Bien différenciée | G3 (> 20 %) |
| Carcinome neuroendocrine
(CNE) |
Peu différenciée (petites ou grandes cellules) | G3 (> 20 %) |
| Néoplasie mixte neuroendocrine/non neuroendocrine
(MiNEN) |
Association d’un contingent neuroendocrine et d’un contingent non neuroendocrine | Tous grades |
________________________________________________________________________________
________________________________________________________________________________
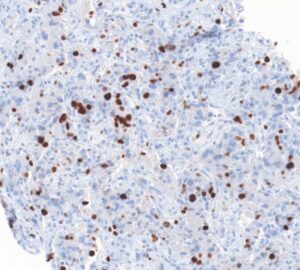
Fig. 1.
TNE pancréatique de grade 3 avec un index de prolifération Ki-67 évalué à 22 %.
Coloration hématoxyline après immunomarquage nucléaire de l’anticorps MIB1. Grossissement × 20.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
III Présentation clinique
Les TNE-DP sont non fonctionnelles dans 80 % des cas et sont alors découvertes fortuitement lors d’une endoscopie, un scanner ou une IRM abdominale.
Dans 20 % des cas, les TNE-DP sont révélées par des symptômes en rapport avec une sécrétion hormonale (tableau 2).
________________________________________________________________________________
Tableau 2.
Caractéristiques des principales TNE-DP fonctionnelles. (Source : CEEDMM, 2021.)
⁎ Cf. Item 240 – Hypoglycémie.
⁎⁎ Cf. Item 244 – Adénome hypophysaire.
| Sécrétion dominante | Nom | Présentation clinique : principaux signes | Marqueur biologique |
| Insuline | Insulinome* | Hypoglycémie organique | Insuline inadaptée à la glycémie basse |
| Gastrine | Gastrinome | Ulcères œso-gastro-duodénaux récidivants, diarrhées résolutives sous IPP | Gastrine élevée + débit acide basal élevé |
| ACTH | Cushing paranéoplasique | Signes de Cushing sévères | Cortisol urinaire des 24 heures élevé
ACTH circulante inadaptée (« normale » ou augmentée) Tests dynamiques** |
| Glucagon | Glucagonome | Diabète, érythème migrateur, diarrhée, amaigrissement, thromboses | Diabète, glucagon circulant élevé |
| VIP | VIPome | Diarrhée hydroélectrolytique profuse, hypokaliémie | VIP élevé |
| GHRH | Acromégalie (exceptionnelle) | GHRH, GH, IGF-1 élevés | |
| Sérotonine | Syndrome carcinoïde | 5-HIAA urinaires élevés |
________________________________________________________________________________
IV Imagerie conventionnelle et fonctionnelle
Une TNE-DP est diagnostiquée par l’endoscopie (fig. 2A). Le scanner TAP injecté (temps artériel et veineux) est l’examen de première intention pour dépister une TNE-P et en faire le bilan d’extension : il est caractéristique par l’intense vascularisation de la tumeur à la phase artérielle précoce (fig. 2B). Il peut être complété par une IRM abdominale pour mieux visualiser les métastases hépatiques et une écho-endoscopie pour faire le bilan d’extension locorégionale et, parfois, affirmer le diagnostic avec une ponction pancréatique (fig. 3).
________________________________________________________________________________
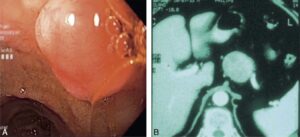
Fig. 2.
TNE du bulbe duodénale en endoscopie responsable d’un syndrome de Zollinger-Ellison (A) et TNE pancréatique visualisée au scanner (B), sécrétant de l’ACTH et responsable d’un syndrome de Cushing paranéoplasique.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
________________________________________________________________________________
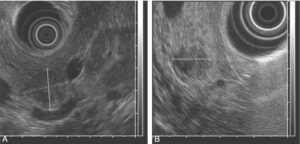
Fig. 3.
TNE du pancréas en écho-endoscopie du corps pancréatique (17 × 19 mm) (A). Notez la boucle de l’artère splénique en arrière de la tumeur. Lésion hypoéchogène de la partie basse de la tête du pancréas (10 mm) (B).
(Source : CEEDMM, 2021.)
________________________________________________________________________________
La place de l’imagerie fonctionnelle (Octréoscan®, TEP DOTA-TOC ou DOTA-NOC) et TEP-FDG (fig. 4) est fondamentale. Elle permet de réaliser le bilan d’extension de la TNE-DP, donne des indications sur le pronostic — une tumeur fixant intensément sur une imagerie des récepteurs de la somatostatine, sans fixation au TEP-FDG, sera de bon pronostic ; inversement, une lésion avec Octréoscan® négatif et TEP-FDG positif sera de mauvais pronostic — et peut être utile à des fins préthérapeutiques (radiothérapie interne vectorisée par analogues de la somatostatine radiomarqués).
________________________________________________________________________________
Formes familiales et syndromes de prédisposition génétique aux TNE-DP
C’est le contexte évocateur de néoplasies multiples qui fait suspecter le diagnostic de néoplasie endocrinienne multiple de type 1 (NEM1) : TNE exclusivement duodénopancréatique, non fonctionnelle, gastrinome ou insulinome, associées à des tumeurs de l’hypophyse et à des adénomes des parathyroïdes.
________________________________________________________________________________
________________________________________________________________________________
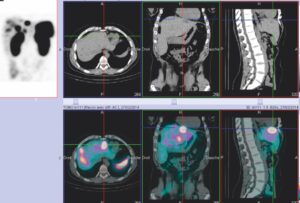
Fig. 4.
Scintigraphie Octréoscan® couplée au scanner (SPECT-CT) chez une femme de 41 ans avec un glucagonome pancréatique métastatique dont la tumeur primitive a été retirée, qui visualise les métastases hépatiques avant un traitement par radiothérapie interne vectorisée.
(Source : CEEDMM, 2021.)
________________________________________________________________________________
________________________________________________________________________________
Points-clés
- Les TNE-DP sont rares.
- Elles se dévoilent parfois par des symptômes endocrines comme les hypoglycémies organiques, un syndrome de Zollinger-Ellison ou un syndrome de Cushing.
- Le diagnostic est souvent posé par le contexte clinico-biologique couplé à l’imagerie conventionnelle et fonctionnelle (principalement celle ciblant les récepteurs de la somatostatine).
________________________________________________________________________________
© CEEDMM – Août 2022.
